電池の容量は(m)Ahという単位で示されます。電流(A)に時間(h)を乗じたものになります。最近ではWhで示されることもありますが、Whについては改めて解説したいと思います。
電池容量は何で決まるかというと材料から取り出せる電荷の数で決まります。電池ではプラスを正極(カソード)、マイナスを負極(アノード)と呼びます。電解の場合は陽極(アノード)と陰極(カソード)なのでややこしいですが、正・負と陰・陽で区別をしています。正極及び負極の材料のことを活物質と呼びます。この活物質の種類と量で容量は決まります。正・負極どちらか少ない方の活物質の持つ容量が電池の容量となります。
判り易い様に金属負極を例にして計算してみましょう。乾電池に使われる亜鉛(Zn)とリチウム電池のリチウム(Li)で1gの金属負極の比容量を算出してみます。
ファラデー定数:1モルの電子が持つ電荷量 96500クーロン/モル
1C(クーロン) = 1A・s = 1/3600Ah
| 負極活物質 | 原子量 | 電子量 | 計算式 | 比容量(Ah/g) |
| Zn2+/Zn | 65.41 | 2 | (96500/65.41)×2/3600 = | 0.820 |
| Li+/Li | 6.94 | 1 | (96500/6.94)/3600 = | 3.862 |
リチウムの比容量は亜鉛の4.7倍になることが判ります。正極も同じ様な方法で比容量が算出されます。電圧と同様材料特有の値となります。理論値なので実際に取り出せる容量は幾らか減少しますが、実用電池でも理論値に近い値が得られています。ナトリウム(Na)とかマグネシウム(Mg)も元素周期表で原子量をチェックすると簡単に計算できると思います。
コストを考える際も電池用の活物質の場合は、重さ(kg)単価ではなくAh単価がより重要となってきます。
電池はアナログチックな技術だと思うのですが、見方を変えると電子レベルの技術なのです。半導体の進化はめざましく、よく比較されることがありますが、電池の場合は既に電子に到達しているため容量アップの選択肢が限られているとも言えるかもしれません。原子量(分子量)は分子側なので、大きな元素や分子は不利になります。原子量の小さな元素や化合物は既に研究し尽くされています。正極には化合物が使われることが多いですが、現状のリチウムイオン電池の正極材の比容量は0.15~0.2Ah/gレベルで凌ぎを削っており、新しい材料の登場が待ち望まれるところです。負極に使われる炭素系負極も0.36Ah/gとリチウム金属と比較すると非常に寂しい数値になってしまいます。
また、多くの活物質は固体ですが、中には液体のものもあります。同じ固体でも金属の場合は板状に加工できますが、多くの化合物は粉末で利用されています。粉末中の結晶も基本的には単結晶ではなく多結晶です。化合物の結晶構造から算出される真密度と実際の粒子の密度、更には活物質粉末に導電剤やバインダーを加えて作製される電極の密度には差が出てきます。限られたスペースの中に電極を詰め込む実用電池では、質量当たりの比容量だけでなく体積も考慮する必要があり、密度の低い(詰まりにくい)化合物は想定した様な容量が得られないこともあります。
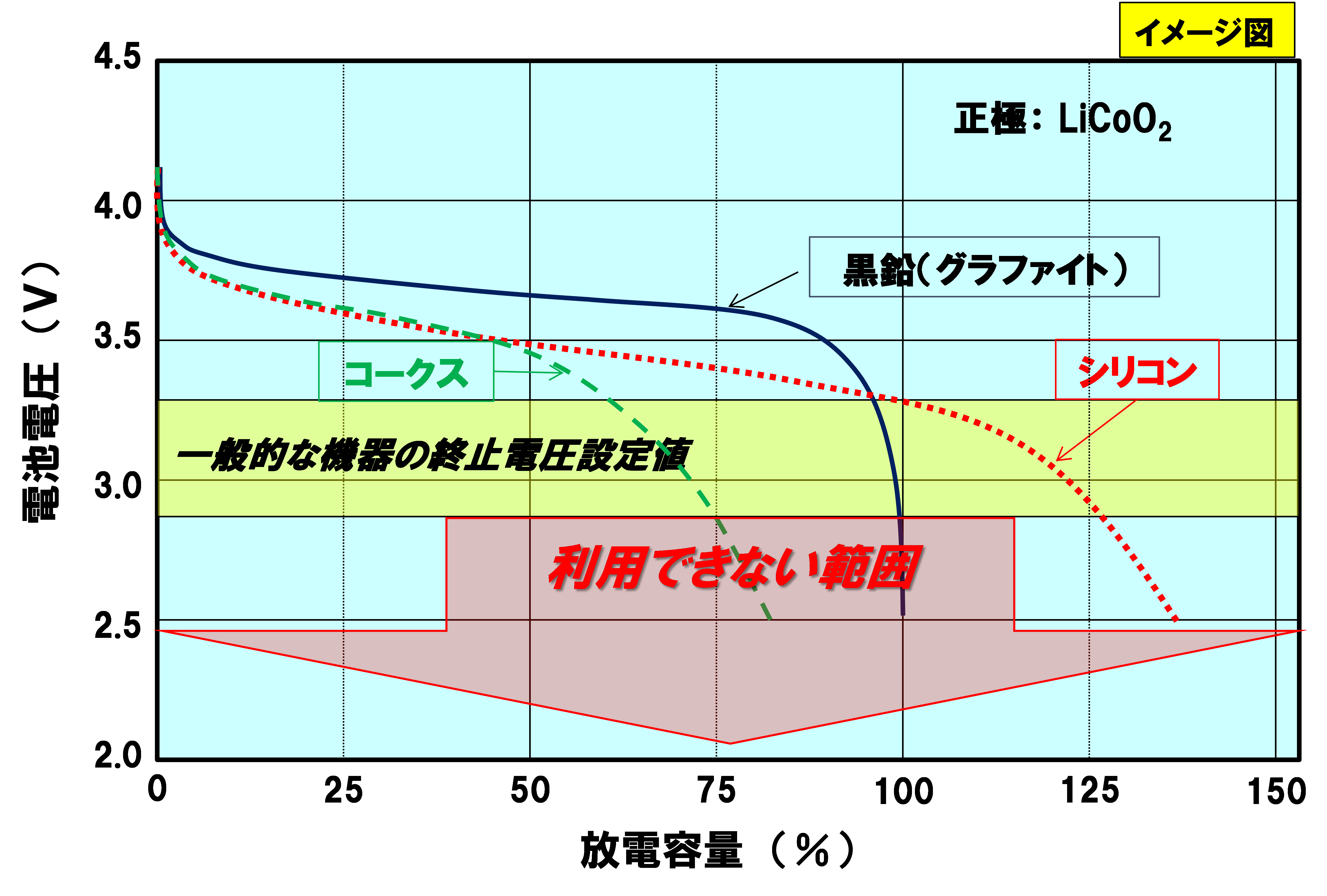
専門的な話になりますが、比容量を計算する際は電池として使える電圧範囲を考慮する必要があります。機器を0Vまで使うことはできません。1.5Vの乾電池で0.9~1.1Vが放電終止電圧になります。
また、万一のことを考えると有害な物質や容易に有害物質を発生させる恐れのある材料は使用できません。乾電池の水銀ゼロ使用も性能低下やコストアップになっても有害物質を使用しないという目的で開発されています。
以上の様に電池の容量を決めるのは電極の活物質であり、電解質は関与しません。比容量は理論値なので電解質(液)の選択を間違うと、理論値を大きく下回ることはあり得ますが、理論容量を超えることはありません。前述の通り、実用化電池でも理論値に近い値が得られており、電解質を変えたところで大幅に容量が増えることはありません。液体でも固体でも同じ話です。
電池の容量は正・負極活物質の持つ比容量に大きく左右されますが、実用化電池では限られたスペースに詰め込む必要があり、単に比容量の差だけでなく色々な工夫をすることにより容量アップが図られています。実使用においてはパッキング技術も重要です。円筒形を角形にするというのも実装面で有利にすることもあり、材料を変えればそれでいいという単純なものではありません。
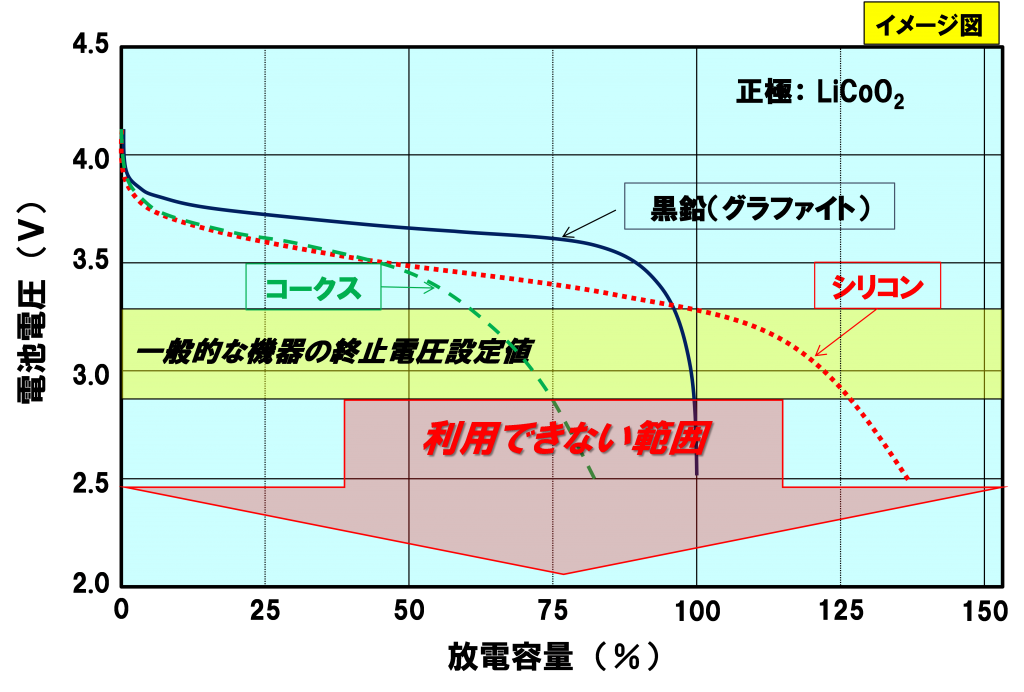
容量と電圧範囲